Phoenixin e hormônios gonadais no controle da homeostase hidromineral
Um novo peptídeo foi recentemente descrito pelo grupo da Dra. Gina Yosten e do Dr. Willis Samson, sendo denominado Phoenixin (PNX). Ele é produzido em muitos tecidos, principalmente no hipotálamo, e demonstrou ser importante no controle da ciclicidade estral, modulando positivamente o eixo hipotalâmico-hipofisário-gonadal. No hipotálamo, o PNX e seu receptor candidato, GPR173, também estão expressos em neurônios magnocelulares do núcleo paraventricular (PVN) e núcleo supraóptico (SON), sugerindo sua participação no controle da homeostase hidromineral por meio do sistema hipotálamo-neuro-hipofisário.
Surpreendentemente, apesar de o PNX ser um peptídeo considerado primariamente reprodutivo, este não está envolvido com a liberação neuro-hipofisária de ocitocina (OT), mas sim apenas de vasopressina (AVP)(1-3). E, embora não haja diferença na liberação de AVP induzida pelo PNX entre fêmeas e machos intactos, foi identificado um potencial elemento responsivo ao estrogênio na via do PNX, sugerindo que os hormônios ovarianos podem modular o PNX. Nesse sentido, fêmeas adultas intactas apresentam maior imunomarcação para o receptor GPR173 no hipotálamo quando comparado com os machos.
Adicionalmente, foi observado que, após a puberdade, as fêmeas apresentam aumento significativo da expressão do RNAm para GPR173 em vários tecidos, como hipófise, ovários e PVN, quando comparado com a fase pré-puberdade. A falência ovariana induzida pela ovariectomia promoveu uma redução significativa da expressão de RNAm para PNX no hipotálamo. Em conjunto, esses dados sugerem que a presença dos hormônios ovarianos é decisiva para a síntese de PNX e seu receptor candidato, GPR173.
Durante a gestação, tanto em mulheres quanto em animais, são observadas alterações na homeostase hidromineral com expansão do volume sanguíneo e baixa osmolalidade associadas a um limiar reduzido para estimulação hiperosmótica da secreção de AVP. Em mulheres, embora a vasopressinase seja responsável pela metabolização da AVP, em certos casos ocorre uma disfunção desse metabolismo, predispondo as mulheres a desenvolver doenças cardiovasculares associadas ao desequilíbrio hidromineral, como hipertensão induzida pela gravidez(4-6).
Os níveis circulantes de esteroides ovarianos aumentam ao longo da gravidez, atingindo valores máximos no final da gestação(6-7). Nesse contexto, foi levantada a hipótese de que os hormônios ovarianos estimulam a síntese e secreção de PNX, bem como a expressão de GPR173, o que é importante para a secreção paradoxal de AVP durante a hipervolemia e hiponatremia observadas durante a gestação. Para testar essa hipótese, avaliamos o conteúdo hipotalâmico de PNX, AVP e expressão de RNAm para GPR173, além da dosagem plasmática de AVP e PNX, ao longo da gestação. Os resultados demonstram um aumento significativo do conteúdo hipotalâmico de PNX, AVP e expressão de RNAm para GPR173 com o progresso da gestação, além de haver uma correlação positiva entre a secreção plasmática de AVP e PNX.
Adicionalmente, foi avaliado o papel do PNX e de seu receptor candidato, GPR173, na ingestão de água em fêmeas e machos intactos, e foi observado que em ambos os sexos o PNX induziu dipsogênese, com maior magnitude nas fêmeas. A resposta dipsogênica do PNX é dependente de seu receptor candidato GPR173, uma vez que seu bloqueio impediu a ação dipsogênica do PNX. Portanto, além de o PNX induzir o aumento da liberação de AVP, que está envolvida com a retenção de água livre corporal e vasoconstrição, esse peptídeo também apresenta um importante papel na indução da ingestão de água.
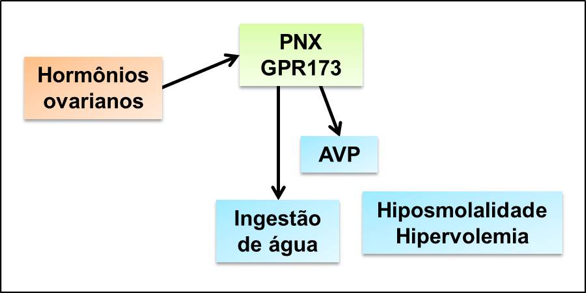
Assim, nosso grupo da FMRP-USP, em parceria com o grupo do Dr. Willis Samson e da Dra. Gina Yosten, da Saint Louis University (EUA), tem demonstrado de forma pioneira que o PNX apresenta um relevante papel no controle da homeostase hidromineral e está sob a regulação positiva dos hormônios ovarianos. Além disso, os dados sugerem que o PNX está envolvido com a liberação paradoxal de AVP diante da hiposmolalidade e hipervolemia observadas durante a gestação. Um importante aspecto desse estudo é a possibilidade de identificar potenciais alvos farmacológicos para prevenção do desenvolvimento de doenças cardiovasculares durante a gravidez.
O trabalho ganhou o Prêmio Melhor Tema Livre Área Básica no COPEM 2021.
Autores:
Gislaine Almeida-Pereira1,2, Christopher J Haddock1, Grant R Kolar1, Gina LC Yosten1, Lucila LK Elias2, José Antunes-Rodrigues2, Willis K Samson1
1Saint Louis University School of Medicine, St Louis, MO, United States
2Medical School of Ribeirão Preto, São Paulo University, FMRP-USP, Brasil
Referências:
imagem: iStock

Comments